Визначаються суттєві зміни в діагностиці раку легені, що впливає на вибір лікування та його результати.
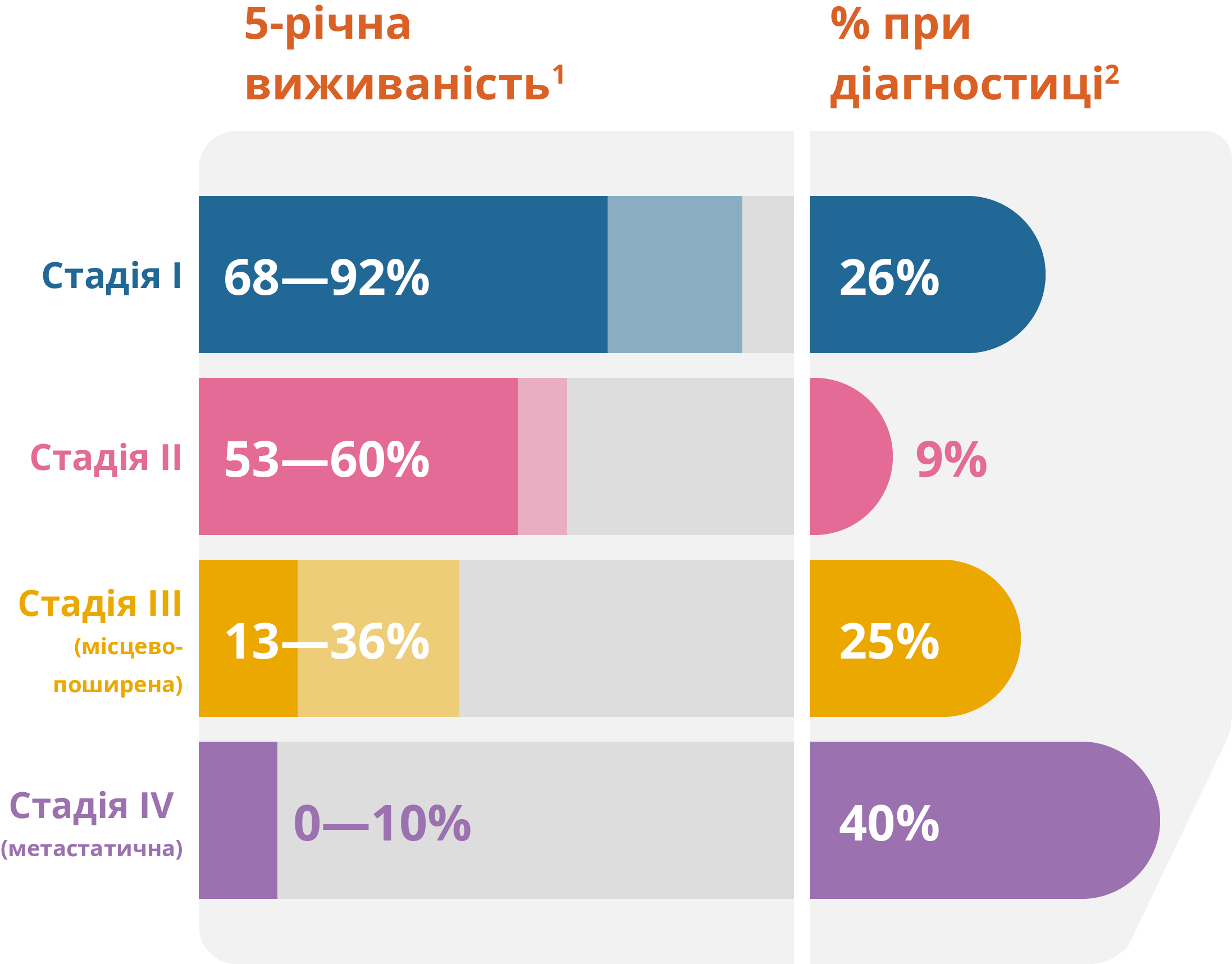
Але кількість хворих з пізніми стадіям (ІІІ-ІV) залишається великою, що впливає на загальні результати лікування1.
В той же час, досягнуті вагомі результати в лікування хворих ІІІ-ІV за останні десятиріччя за рахунок впровадження в терапію таргетних препаратів та імунотерапії 8-10.
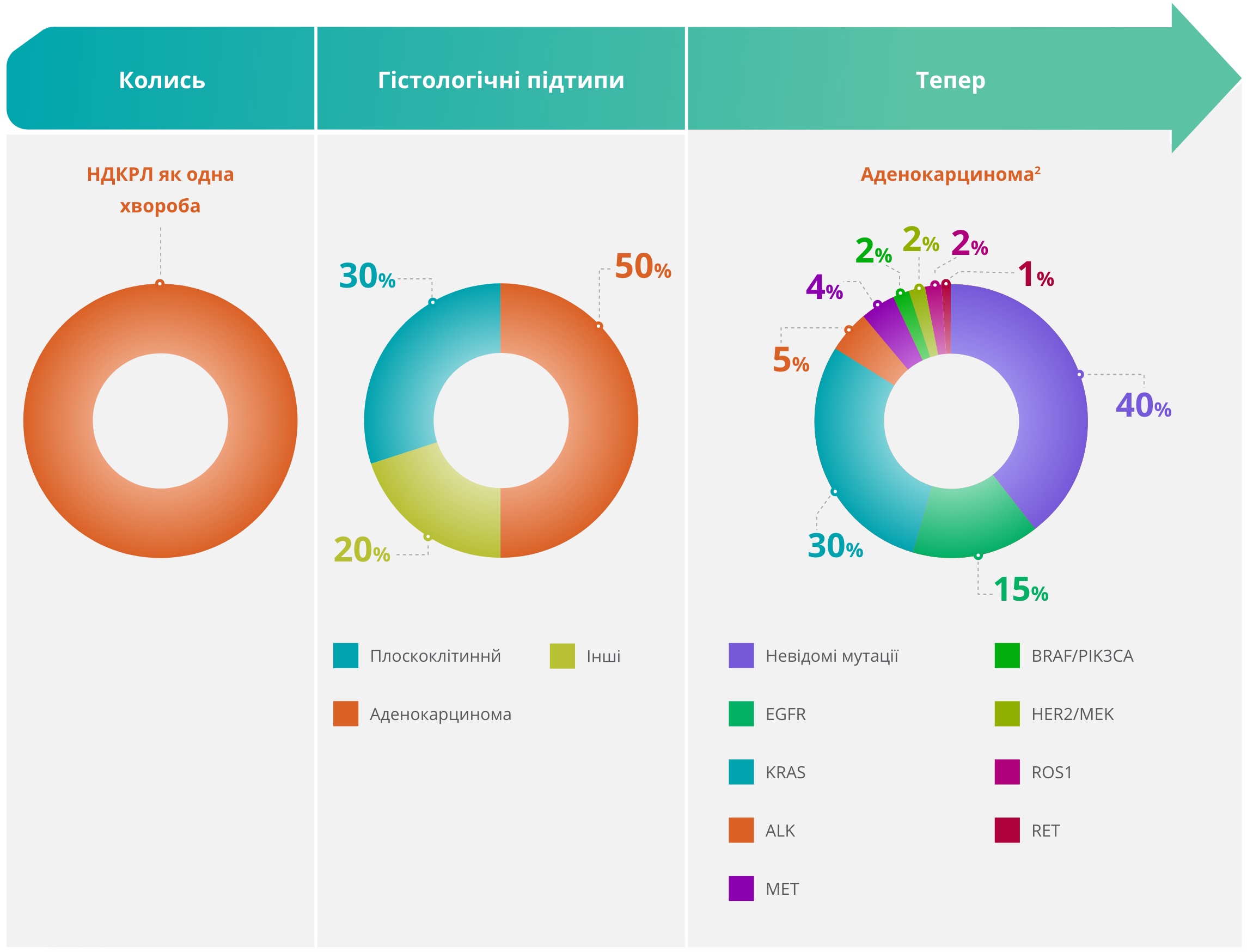
Колись недрібноклітинний рак легені (НДКРЛ) розглядали як одне захворювання, але з розвитком молекулярних методів діагностики стало зрозуміло, що це багато різних патологій! 2.
Рак легені: Захворюваність та 5‑річна виживаність1
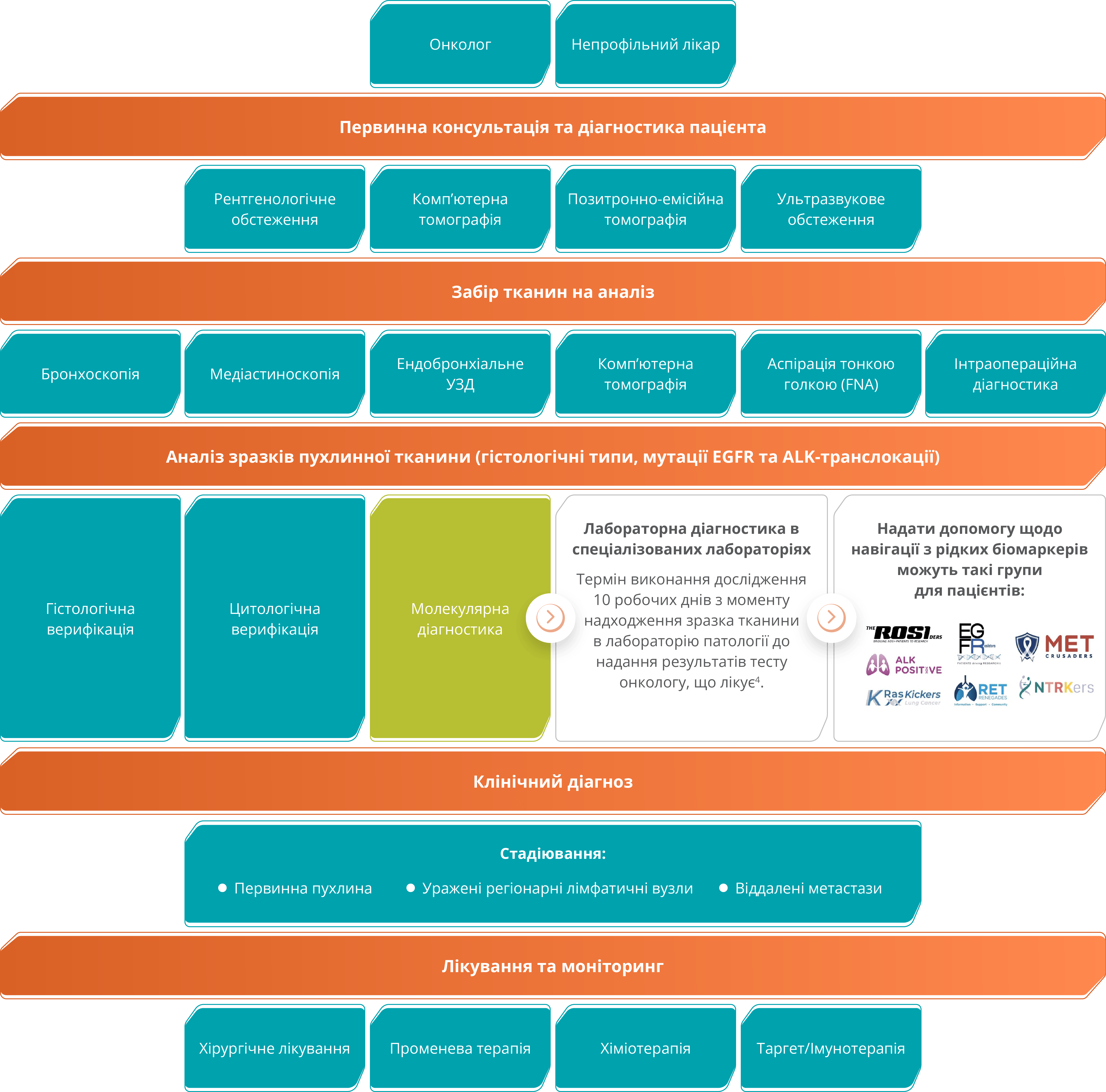
Маршрут пацієнта з раком легені3
Рекомендації настанов: значення ALK-тестування у діагностиці

AMP — Association for Molecular Pathology (Асоціація молекулярної патології); CAP — College of American Pathologists (Коледж американських патологів); ESMO — European Society for Medical Oncology (Європейське товариство медичної онкології); IASLC - International Association for the Study of Lung Cancer (Міжнародна асоціація з дослідження раку легені); NCCN ® — National Comprehensive Cancer Network ® (Національна мережа по впровадженню знань в області онкології ®).
a NCCN для NSCLC надають рекомендації щодо певних окремих біомаркерів, які слід протестувати, і рекомендують методи тестування, але не схвалюють будь-які конкретні комерційно доступні аналізи біомаркерів або комерційні лабораторії. NCCN не надає жодних гарантій щодо контенту, його використання чи застосування та відмовляється від будь-якої відповідальності за застосування чи використання будь-яким способом.


Чутливість методів молекулярного тестування при НДКРЛ8
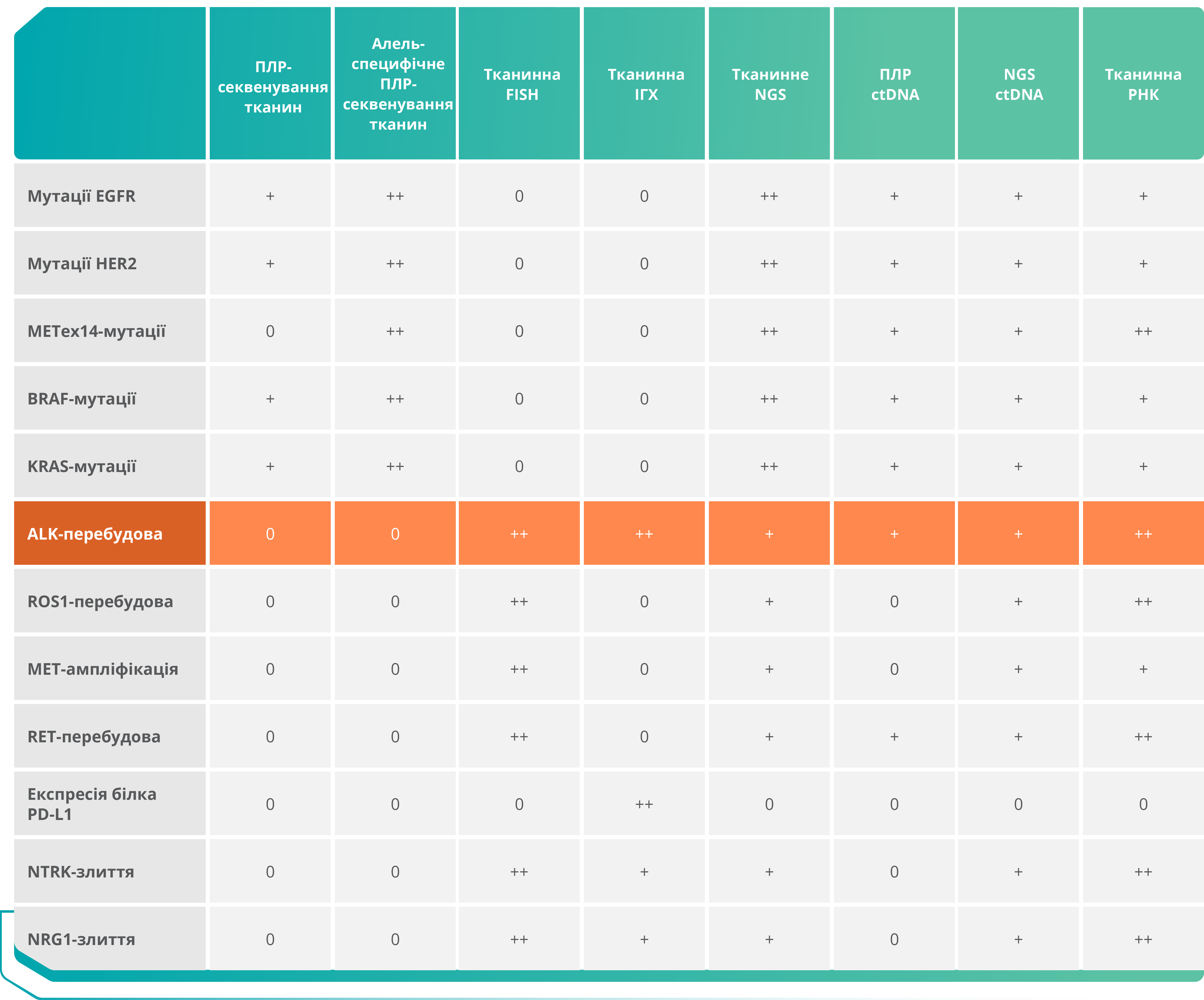
++: Найвища чутливість
+: Нижча чутливість (більша ймовірність хибнонегативного результату)
0: Неефективний метод
EGFR — рецептор епідермального фактора росту; HER2 — рецептор епідермального фактора росту людини 2; ALK — кіназа анапластичної лімфоми; ПЛР — полімеразна ланцюгова реакція; PD-L1 — запрограмована смерть клітини-ліганд 1; NTRK — тирозинкіназа нейротрофічного рецептора; NRG1 — нейрегулін 1; FISH — флуоресцентна гібридизація in situ; IГХ — імуногістохімія; NGS — секвенування наступного покоління; ctDNA — циркулююча ДНК пухлини.
Основні методи ALK-тестування
Методи тестування, визнані діючими рекомендаціями4-7:
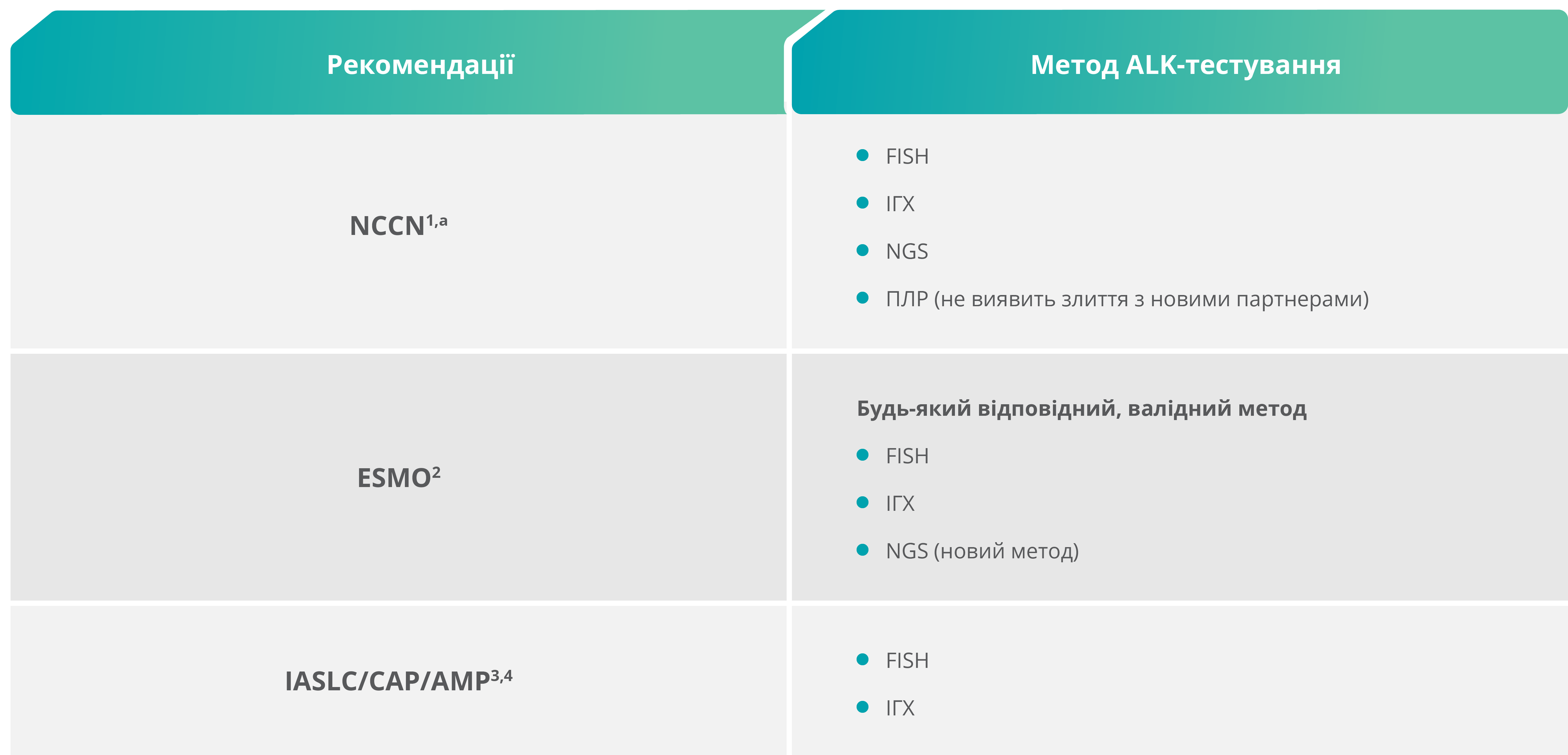
a NCCN не надає жодних гарантій щодо контенту, його використання чи застосування та відмовляється від будь-якої відповідальності за застосування чи використання будь-яким способом.


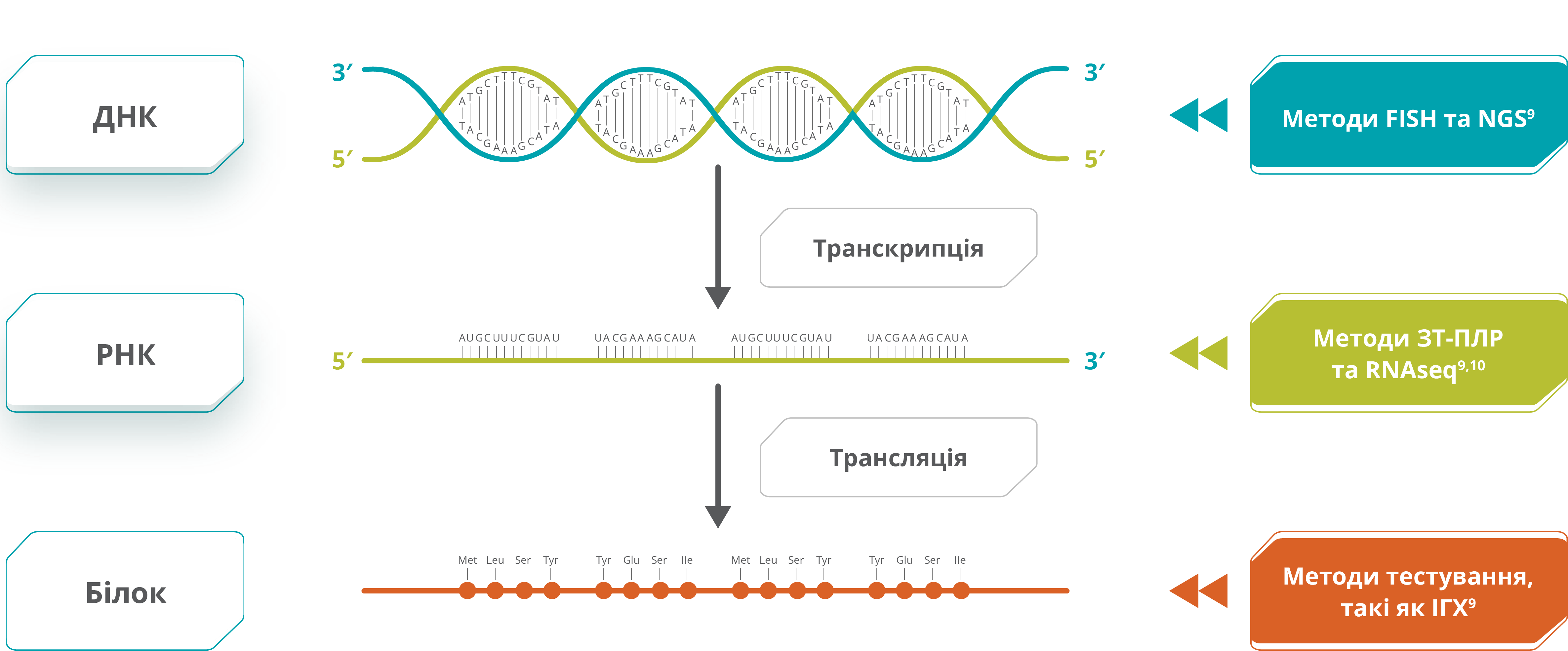


Традиційні методи ALK-тестування
Флуоресцентна гібридизація in situ (FISH)
FISH-зонди, що розділяються, призначені для виявлення злиття генів у результаті між- та внутрішньохромосомних транслокацій9
- Кількісний аналіз може виявити перегрупування, навіть якщо партнер по злиттю невідомий
FISH-зонд маркує різні кінці точок злиття двома флуохромами (1 зелений, 1 червоний)9
- Кольори розділяються, якщо ген перебудований, тобто ALK-позитивний (5’-делеція також може відбуватися під час перегрупування ALK; зразки із втратою сигналу 5'-зонда вважаються позитивними щодо ALK-перегрупування)3,9
- Кольори зливаються (або є у вигляді єдиного жовтого сигналу), якщо зразок негативний щодо перебудов ALK9
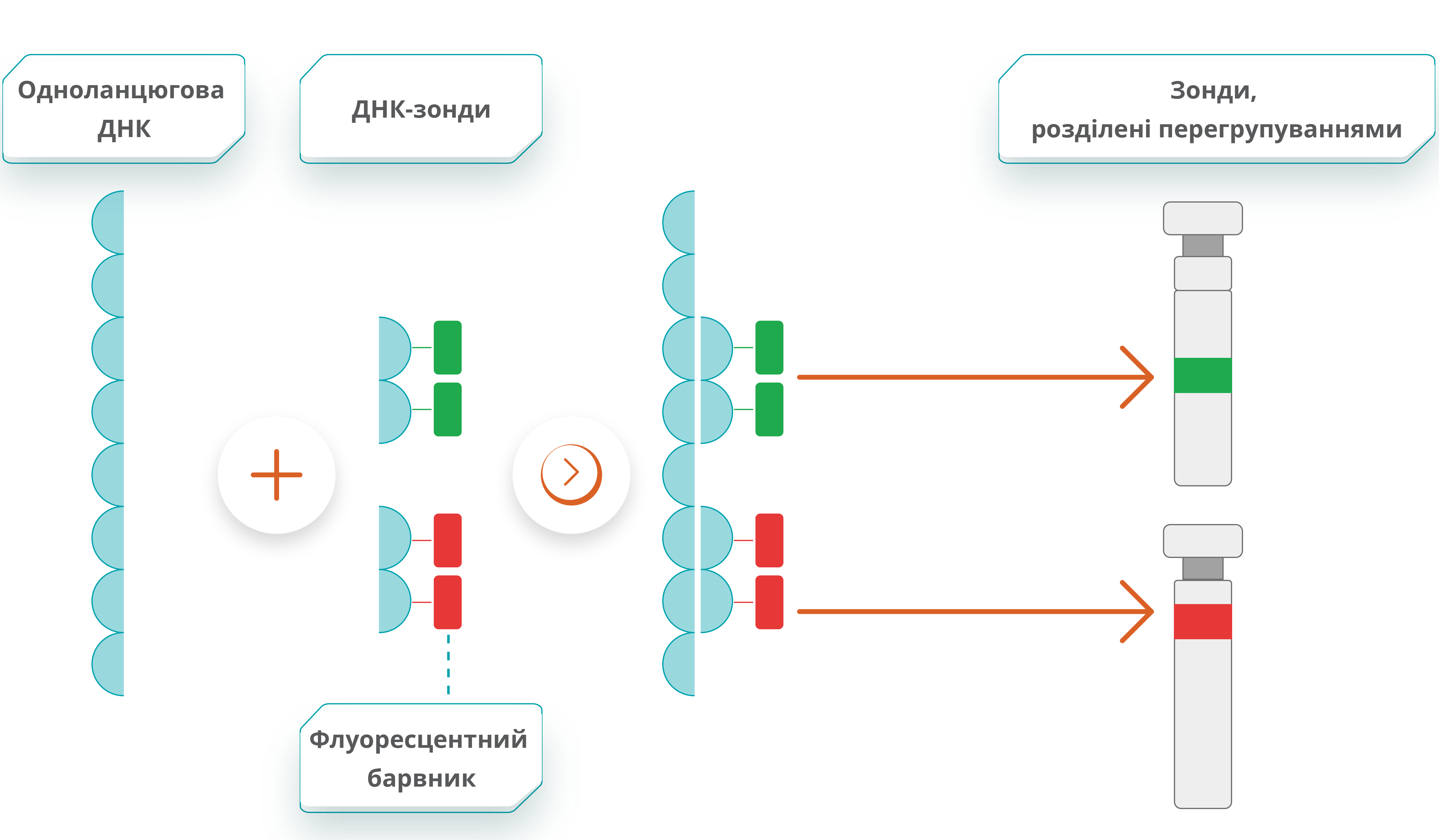


ALK-тестування методом FISH9
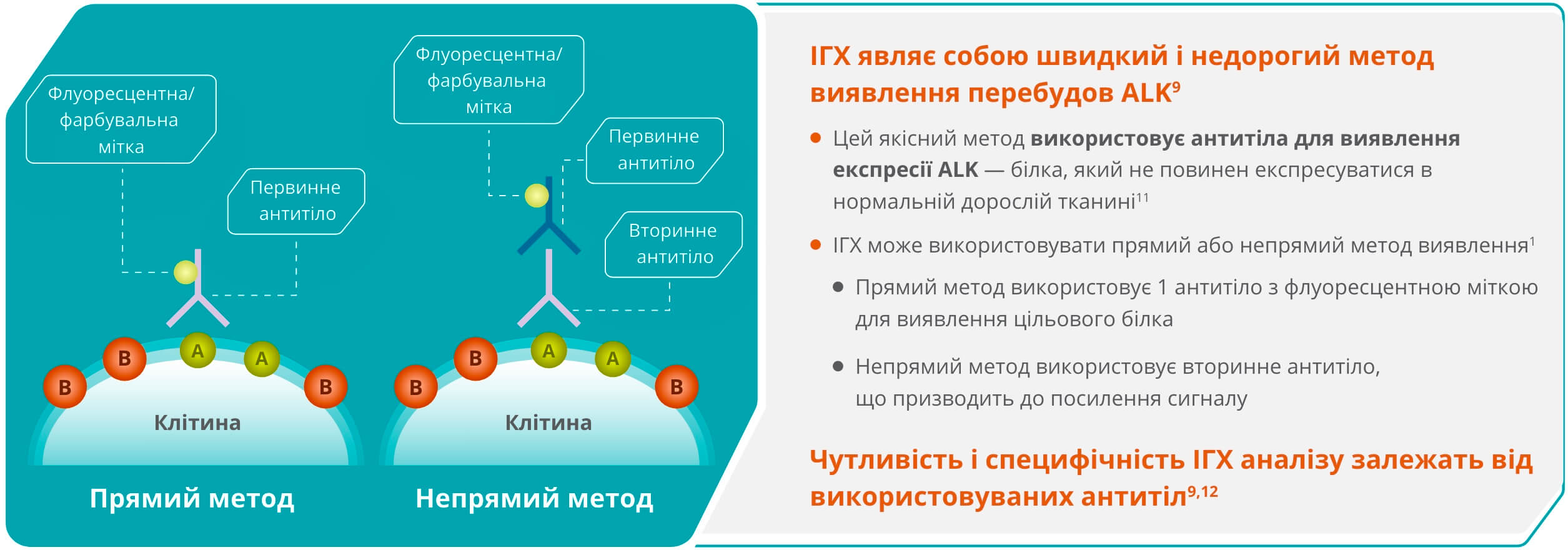
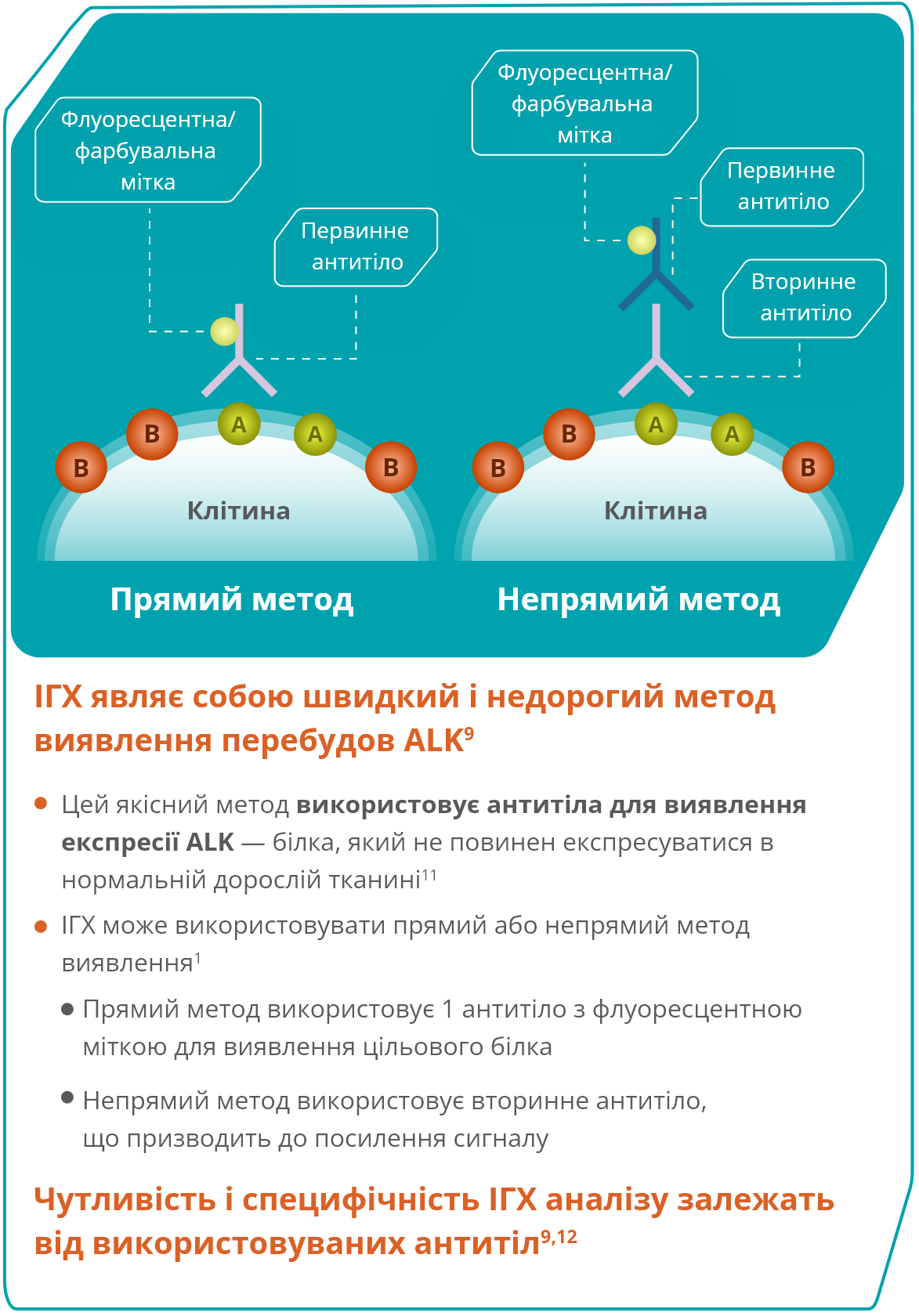
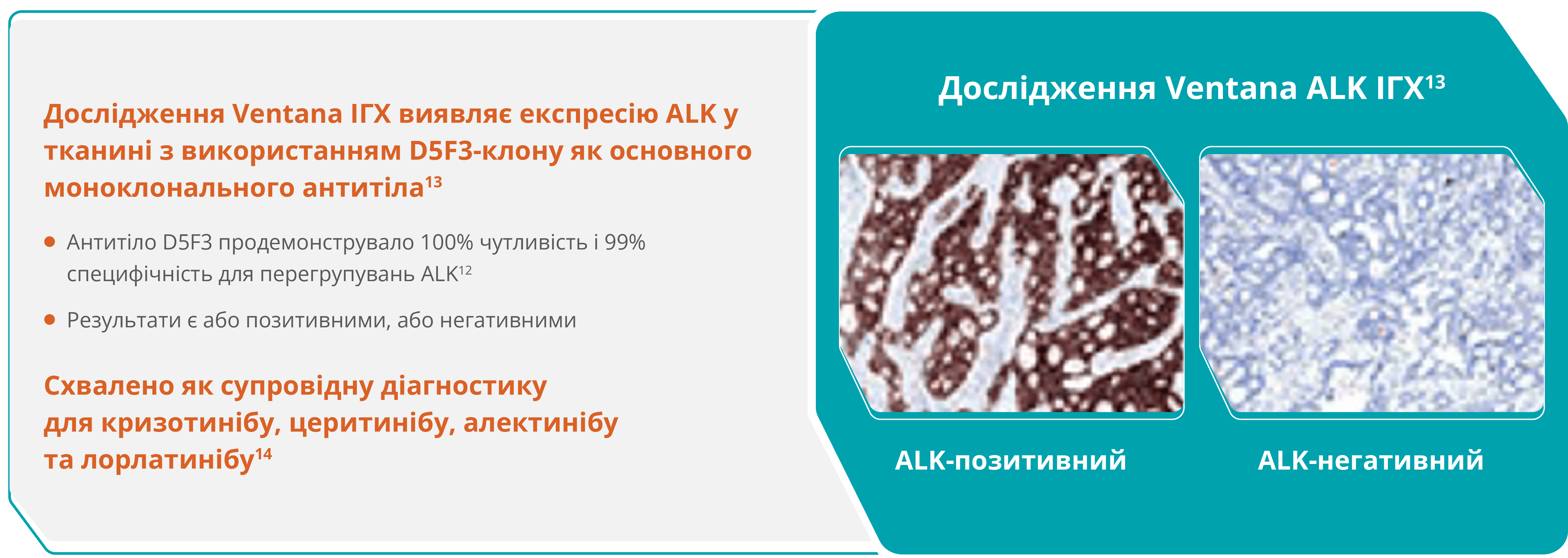
Імуногістохімія (ІГХ)
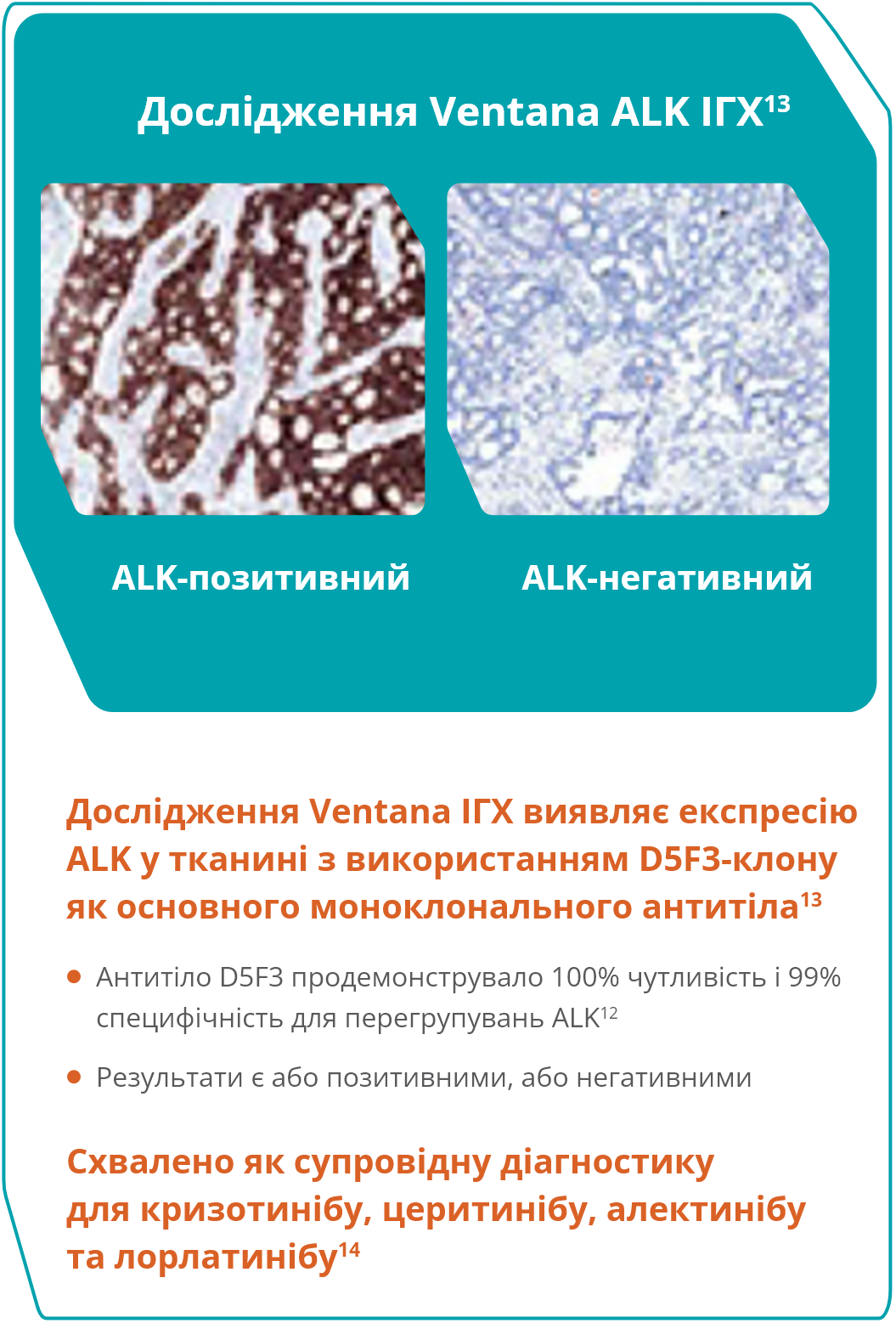
Новий метод ALK-детекції
ПЛР


a У рекомендаціях NCCN згадується ПЛР у реальному часі, а не ЗТ-ПЛР; однак є більше повідомлень щодо застосування ЗТ-ПЛР у ALK-тестуванні. NCCN не надає жодних гарантій щодо контенту, його використання чи застосування та відмовляється від будь-якої відповідальності за застосування чи використання будь-яким способом.
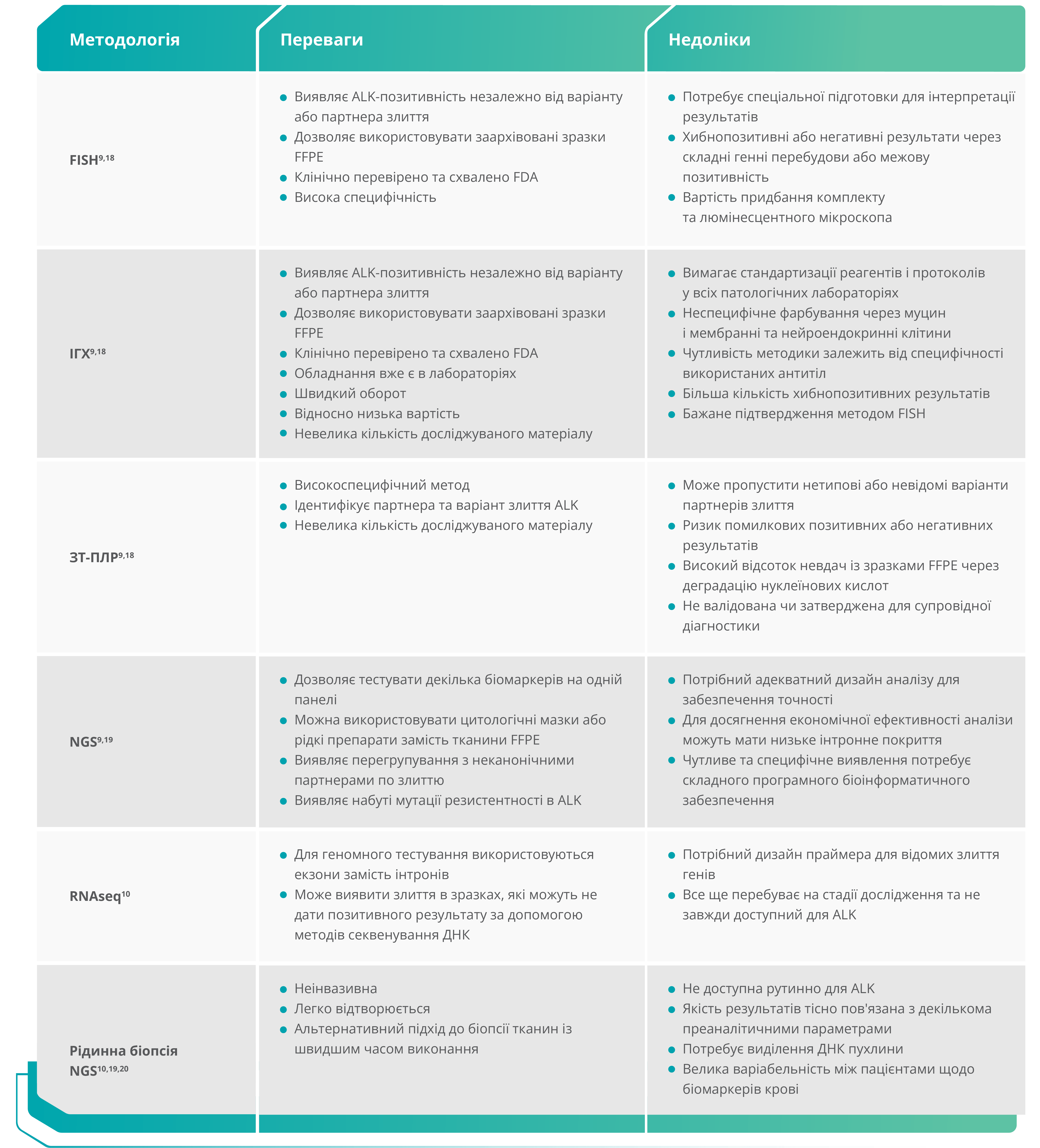
Переваги та недоліки поточних методів діагностики ALK
Висновки:
-
Перебудови ALK є драйверними мутаціями при НДКРЛ, які активують низхідні онкогенні сигнальні шляхи
-
Керівництва NCCN, ESMO та IASLC/CAP/AMP для НДКРЛ рекомендують проводити тестування на перебудову ALK при діагностиці поширеного НДКРЛa
- Для прогресуючого перебігу захворювання керівництва наразі не містять рекомендацій щодо тестування на ALK-мутації
a NCCN для NSCLC надають рекомендації щодо певних окремих біомаркерів, які слід протестувати, і рекомендують методи тестування, але не схвалюють будь-які конкретні комерційно доступні аналізи біомаркерів або комерційні лабораторії. NCCN не надає жодних гарантій щодо контенту, його використання чи застосування та відмовляється від будь-якої відповідальності за застосування чи використання будь-яким способом.
-
FISH та ІГХ є традиційними методами тестування ALK у пацієнтів з НДКРЛ
- ЗТ-ПЛР та NGS є новими методами, і RNAseq перебуває у розробці
- Рідинна біопсія, яка використовує аналіз мутацій на основі крові замість біопсії тканини, є новим методом виявлення
- Дослідження «The Vysis FISH assay», «Ventana ІГХ assay» та «FoundationOne» на основі NGS є схваленими супровідними діагностичними методами ALK-тестування при НДКРЛ
-
Незважаючи на рекомендації керівництв, частота тестування на ALK є субоптимальною — приблизно 33% пацієнтів у Сполучених Штатах не проходять тестування на ALK, тоді як в інших країнах цей показник варіює
- Проблеми з тестуванням включають вартість, тривалий час для отримання результатів і труднощі зі зразками тканин
- Затримки в тестуванні чи отриманні результатів, або ж повна відсутність тестування може призвести до затримки належного лікування та потенційного погіршення результатів
- Пацієнти з позитивним результатом тесту на перебудову ALK мають більше можливостей отримати таргетну терапію та мати кращі результати
- Goldstraw P, Chansky K, Crowley J, Rami-Porta R, Asamura H, Eberhardt WE, Nicholson AG, Groome P, Mitchell A, Bolejack V; International Association for the Study of Lung Cancer Staging and Prognostic Factors Committee, Advisory Boards, and Participating Institutions; International Association for the Study of Lung Cancer Staging and Prognostic Factors Committee Advisory Boards and Participating Institutions. The IASLC Lung Cancer Staging Project: Proposals for Revision of the TNM Stage Groupings in the Forthcoming (Eighth) Edition of the TNM Classification for Lung Cancer. J Thorac Oncol. 2016 Jan;11(1):39-51. doi: 10.1016/j.jtho.2015.09.009. Link: https://www.jto.org/article/S1556-0864(15)00017-9/fulltext
- Chan BA, Hughes BG. Targeted therapy for non-small cell lung cancer: current standards and the promise of the future. Transl Lung Cancer Res. 2015 Feb;4(1):36-54. doi: 10.3978/j.issn.2218-6751.2014.05.01. Link: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4367711/
- Levy BP, Chioda MD, Herndon D, Longshore JW, Mohamed M, Ou SH, Reynolds C, Singh J, Wistuba II, Bunn PA Jr, Hirsch FR. Molecular Testing for Treatment of Metastatic Non-Small Cell Lung Cancer: How to Implement Evidence-Based Recommendations. Oncologist. 2015 Oct;20(10):1175-81. doi: 10.1634/theoncologist.2015-0114. Link: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4591939/
- Lindeman NI, Cagle PT, Beasley MB, Chitale DA, Dacic S, Giaccone G, Jenkins RB, Kwiatkowski DJ, Saldivar JS, Squire J, Thunnissen E, Ladanyi M. Molecular testing guideline for selection of lung cancer patients for EGFR and ALK tyrosine kinase inhibitors: guideline from the College of American Pathologists, International Association for the Study of Lung Cancer, and Association for Molecular Pathology. Arch Pathol Lab Med. 2013 Jun;137(6):828-60. doi: 10.5858/arpa.2012-0720-OA. Link: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4162344/
- Ettinger DS, Wood DE, Aisner DL, Akerley W, Bauman JR, Bharat A, Bruno DS, Chang JY, Chirieac LR, D'Amico TA, DeCamp M, Dilling TJ, Dowell J, Gettinger S, Grotz TE, Gubens MA, Hegde A, Lackner RP, Lanuti M, Lin J, Loo BW, Lovly CM, Maldonado F, Massarelli E, Morgensztern D, Ng T, Otterson GA, Pacheco JM, Patel SP, Riely GJ, Riess J, Schild SE, Shapiro TA, Singh AP, Stevenson J, Tam A, Tanvetyanon T, Yanagawa J, Yang SC, Yau E, Gregory K, Hughes M. Non-Small Cell Lung Cancer, Version 3.2022, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw. 2022 May;20(5):497-530. doi: 10.6004/jnccn.2022.0025. Link: https://jnccn.org/view/journals/jnccn/20/5/article-p497.xml
- Planchard D, Popat S, Kerr K, Novello S, Smit EF, Faivre-Finn C, Mok TS, Reck M, Van Schil PE, Hellmann MD, Peters S; ESMO Guidelines Committee. Metastatic non-small cell lung cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2018 Oct 1;29(Suppl 4):iv192-iv237. doi: 10.1093/annonc/mdy275. Link: https://www.annalsofoncology.org/article/S0923-7534(19)31710-7/fulltext
- Lindeman NI, Cagle PT, Aisner DL, Arcila ME, Beasley MB, Bernicker EH, Colasacco C, Dacic S, Hirsch FR, Kerr K, Kwiatkowski DJ, Ladanyi M, Nowak JA, Sholl L, Temple-Smolkin R, Solomon B, Souter LH, Thunnissen E, Tsao MS, Ventura CB, Wynes MW, Yatabe Y. Updated Molecular Testing Guideline for the Selection of Lung Cancer Patients for Treatment With Targeted Tyrosine Kinase Inhibitors: Guideline From the College of American Pathologists, the International Association for the Study of Lung Cancer, and the Association for Molecular Pathology. J Mol Diagn. 2018 Mar;20(2):129-159. doi: 10.1016/j.jmoldx.2017.11.004. Link: https://www.jmdjournal.org/article/S1525-1578(17)30590-1/fulltext
- Sequist L V. Personalized, genotype-directed therapy for advanced non-small cell lung cancer. UpToDate. This topic last updated: Sep 26, 2023. Link: https://sso.uptodate.com/contents/image?imageKey=ONC/111926&topicKey=ONC/16538&source=outline_link
- Tsao MS, et al, eds. IASLC Atlas of ALK and ROS1 Testing in Lung Cancer. Aurora, CO: IASLC Press; 2017; Link: https://www.iaslc.org/research-education/publications-resources-guidelines/iaslc-atlas-alk-and-ros1-testing-lung-cancer
- Benayed R, Offin M, Mullaney K, Sukhadia P, Rios K, Desmeules P, Ptashkin R, Won H, Chang J, Halpenny D, Schram AM, Rudin CM, Hyman DM, Arcila ME, Berger MF, Zehir A, Kris MG, Drilon A, Ladanyi M. High Yield of RNA Sequencing for Targetable Kinase Fusions in Lung Adenocarcinomas with No Mitogenic Driver Alteration Detected by DNA Sequencing and Low Tumor Mutation Burden. Clin Cancer Res. 2019 Aug 1;25(15):4712-4722. doi: 10.1158/1078-0432.CCR-19-0225. Link: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6679790/
- Grande E, Bolós MV, Arriola E. Targeting oncogenic ALK: a promising strategy for cancer treatment. Mol Cancer Ther. 2011 Apr;10(4):569-79. doi: 10.1158/1535-7163.MCT-10-0615. Link: https://aacrjournals.org/mct/article/10/4/569/168521/Targeting-Oncogenic-ALK-A-Promising-Strategy-for
- Wynes MW, Sholl LM, Dietel M, Schuuring E, Tsao MS, Yatabe Y, Tubbs RR, Hirsch FR. An international interpretation study using the ALK IHC antibody D5F3 and a sensitive detection kit demonstrates high concordance between ALK IHC and ALK FISH and between evaluators. J Thorac Oncol. 2014 May;9(5):631-8. doi: 10.1097/JTO.0000000000000115. Link: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4186652/
- Ventana Medical Systems. Ventana ALK (D5F3) CDx assay. Accessed April 7, 2021; Link: https://www.accessdata.fda.gov/cdrh_docs/pdf14/P140025c.pdf
- FDA. Accessed April 7, 2021. https://www.fda.gov/medical-devices/vitro-diagnostics/list-cleared-or-approved-companion-diagnostic-devices-vitro-and-imaging-tools
- Teixidó C, Karachaliou N, Peg V, Gimenez-Capitan A, Rosell R. Concordance of IHC, FISH and RT-PCR for EML4-ALK rearrangements. Transl Lung Cancer Res. 2014 Apr;3(2):70-4. doi: 10.3978/j.issn.2218-6751.2014.02.02. Link: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4367661/
- Thermo Fisher Scientific. Accessed April 7, 2021. https://www.thermofisher.com/us/en/home/references/ambion-tech-support/rtПЛР-analysis/general-articles/rt--ПЛР-the-basics.html
- Sigma-Aldrich. Accessed April 7, 2021. https://www.sigmaaldrich.com/life-science/molecular-biology/ПЛР/ЗТ-ПЛР.printerview.html
- Weickhardt, A.J., Aisner, D.L., Franklin, W.A., Varella-Garcia, M., Doebele, R.C. and Camidge, D.R. (2013), Diagnostic assays for identification of anaplastic lymphoma kinase-positive non–small cell lung cancer. Cancer, 119: 1467-1477. https://doi.org/10.1002/cncr.27913. Link: https://acsjournals.onlinelibrary.wiley.com/doi/full/10.1002/cncr.27913
- Mok TS, et al, eds. IASLC Atlas of EGFR Testing in Lung Cancer. Aurora, CO: IASLC Press; 2017; Link: https://www.iaslc.org/research-education/publications-resources-guidelines/iaslc-atlas-egfr-testing-lung-cancer-guidebook
- Hofman, P. Liquid Biopsy and Therapeutic Targets: Present and Future Issues in Thoracic Oncology. Cancers 2017, 9, 154. https://doi.org/10.3390/cancers9110154. Link: https://www.mdpi.com/2072-6694/9/11/154




